UL001
ICH-Q3Dガイドライン対応試験(医薬品中の元素不純物測定)
医薬品はその特性上、品質管理が極めて重要な為、各種規制により厳しく管理されています。近年、医薬品製造触媒の多様化や分析技術の発展などの背景から、金属元素不純物の品質管理が見直されています。そのような中、日本においても医薬品元素不純物ガイドラインとして、平成27年9月30日付で「薬食審査発0930第4号」が発出され、ICH-Q3Dが施行されました。ガイドラインの適用対象は、平成29年4月1日以降に承認申請される新医薬品(新製剤)ですが、今後既存製剤への適用も検討されています。
弊社は、超微量分析対応の環境・設備を保有し、多種多様な材料における超微量金属分析について豊富な実績・経験を有しています。これら設備面・経験面の長所を活かして、ICH-Q3D試験の受託にも対応しています。
ご依頼の流れ
- お問い合わせ・ご相談
-
- 分析に必要な情報の確認(試料形態、対象元素、定量下限値の設定など)
- 見積書のご提示(信頼性保証の有無などにより、費用変動)
-

- 予備試験
-
- 前処理条件の検討(分解法・分解時間・分解液の選定など)
- 試験条件の評価(元素の概算濃度、夾雑元素確認、添加回収など)
-

- バリデーション
-
- システム適合性(特異性、直線性、再現性、併行精度、検出限界など)の評価
-

- 試験計画書、記録書の作成・承認
-
- 試験計画書、記録書の作成と承認
-

- 本試験
-
- 試験計画書内容に基づき、本試験実施
-

- ご報告
-
- 速報をメールにてご連絡
- 報告書草案をご確認頂いた後、QAを実施し、最終化
ハード面での優位性

クリーンルーム内の様子
装置は高分解能誘導結合型プラズマ質量分析(HR-ICP-MS)
- クリーンルーム内で
前処理・測定が可能 
- 汚染を最大限排除可能

- 信頼性の高い測定が可能
ソフト面での優位性
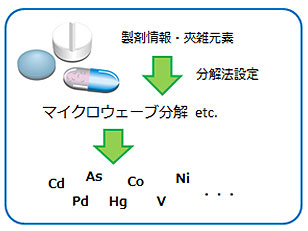
- 分解ノウハウが豊富

- 分解法の設定が的確

- 精緻で迅速な分析が可能
これまで培ってきた超微量金属分析の豊富な経験

ICH-Q3D対応試験も受託可能